电话:028-88610620
邮箱:pr@keymedbio.com/BD@keymedbio.com
简历投递:HR-kny@keymedbio.com
2022年3月29日,中国成都——康诺亚生物医药科技有限公司(香港联交所股份代码:02162)发布2021年度公司业绩报告。

业绩速览
产品管线
■ 核心产品CM310(IL-4Ra抗体)启动并完成中重度特应性皮炎适应症IIb期临床试验,于2021年11月公布该临床数据,截至业绩公告发布日已进入临床III期;
■ 核心产品CM326(TSLP抗体)启动并完成I期健康人试验,该项试验结果已于2021年11月公布。目前,已启动CM326针对成人中重度特应性皮炎Ib/IIa期临床试验;即将启动针对慢性鼻窦炎伴鼻息肉的Ib/IIa期临床试验;
■ 核心产品CMG901(Claudin 18.2 抗体偶联药物)于2021年持续推进实体瘤受试者I期临床试验,计划于2022年Q2启动剂量拓展阶段;已于2021年3月取得FDA针对胃及胃食管连接部癌症I期临床试验许可;
■ 核心产品CM313(CD38抗体)于2021年启动并推进复发╱难治性多发性骨髓瘤及淋巴瘤等血液系统恶性肿瘤适应症I期临床试验,该项试验剂量递增阶段预计将于2022年H1完成。同时,已于2022年Q1启动CM313剂量拓展阶段试验;2022年1月提交CM313 SLE适应症IND申请。
产能扩建
■ 新生产基地一期建设封顶并启动机电安装,将提供16,000升产能。
财务业绩&资本市场表现
■ 2021财年对外合作累计收入1.1亿人民币,研发投入3.6亿人民币,同比增长181%。公司在手现金约35亿人民币,可充分支持公司未来发展;
■ 2021年7月8日,康诺亚于港交所主板上市,股票代码2162.HK。
产品管线快速推进 核心产品成绩亮眼
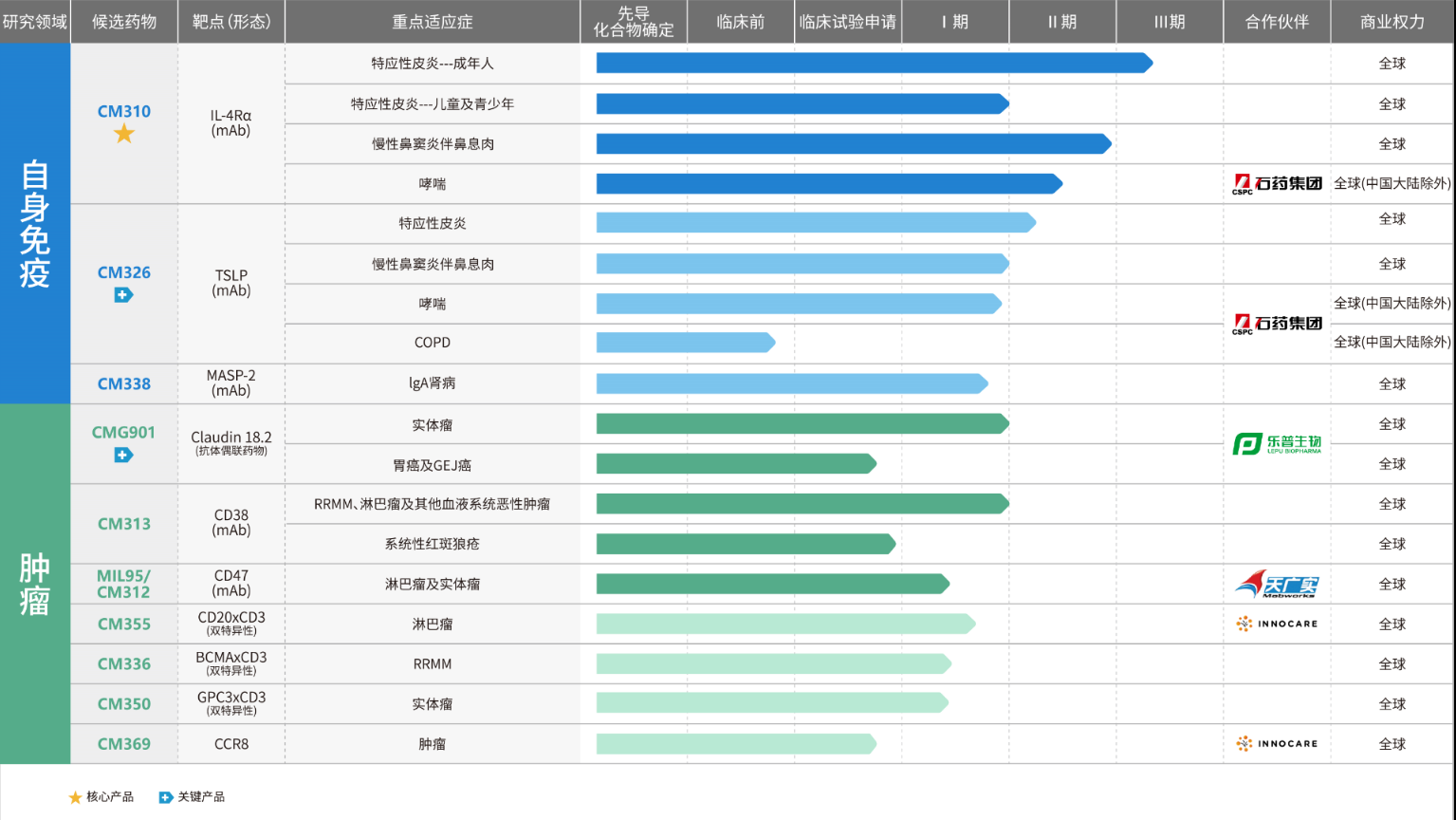
*康诺亚产品管线进度(截至2021年业绩公告发布日)
2021年及近期管线亮点——
CM310(IL-4Rα抗体)
CM310是国内首个国产进入临床研究的该靶点药物,拟用于中重度特应性皮炎、中重度哮喘、慢性鼻窦炎伴鼻息肉等疾病治疗。
■ 2021年11月已完成CM310成人中重度特应性皮炎IIb期临床研究,获得积极数据结果,显示出CM310优异的疗效与安全性。公司已于2022年Q1启动针对成人中重度特应性皮炎的III期临床研究;
■ 2021年H1启动针对慢性鼻窦炎伴鼻息肉的II期临床试验,并计划于2022年H2启动该适应症的III期临床研究申请;
■ 2021年5月获得国家药品监督管理局批准,开展中重度哮喘II期临床试验;
■ 2021年10月获得国家药品监督管理局批准,开展针对儿童及青少年中重度特应性皮炎的临床试验。
CM326(TSLP抗体)
CM326为中国第一、世界第二个进入临床研究阶段的该靶点抗体药物,拟用于中重度特应性皮炎、中重度哮喘、慢性鼻窦炎伴鼻息肉等疾病治疗,有潜力与CM310形成协同效应。
■ 2021年3月获得国家药品监督管理局批准,开展中重度哮喘的临床试验;
■ 公司已于2021年11月完成CM326面向健康志愿者的Ia期临床研究;
■ 2021年11月获得国家药品监督管理局批准,开展中重度特应性皮炎及慢性鼻窦炎伴鼻息肉的临床试验。2022年初已启动CM326治疗中重度特应性皮炎患者的Ib/IIa期临床试验,慢性鼻窦炎伴鼻息肉适应症的Ib/IIa期临床试验也即将开展。
CMG901(Claudin 18.2抗体偶联药物)
CMG901是世界首创针对Claudin18.2的抗体偶联药物,拟用于胃癌、胰腺癌等实体瘤治疗。临床前安全性研究表明,CMG901药效佳、安全性好。
■ 目前即将完成实体瘤I期临床剂量爬坡试验,预计于2022年Q2初启动剂量拓展阶段试验;
■ 2021年3月,获得美国FDA批准开展CMG901针对胃及胃食管连接部癌症I期临床试验。
CM313(CD38抗体)
CM313是中国首款获批IND的国产CD38抗体药物。鉴于在临床前研究中的疗效可观,CM313有望成为复发/难治性多发性骨髓瘤、淋巴瘤及其他血液系统恶性肿瘤患者的创新型治疗选择。
■ 于2021年H1启动剂量递增临床试验,剂量拓展阶段试验已于2022年Q1末启动;
■ CM313治疗系统性红斑狼疮(SLE)适应症IND申请已于2022年1月提交。
3款双抗产品
康诺亚3款双抗候选药物CM355(CD20xCD3)、CM336(BCMAxCD3)、CM350(GPC3xCD3)均获进展。
■ CM355于2021年9月获得针对治疗复发/难治性非霍奇金淋巴瘤的IND批准,已于2022年1月完成首名患者给药;
■ CM336、CM350已获批IND,预计将于2022年Q2启动I期临床首例受试者给药。
新披露在研新药——CM369
CM369是一种抗趋化因子受体8(CCR8)单克隆抗体,是康诺亚和诺诚健华共同开发的潜在first-in-class药物,可作为单一疗法或与其他疗法联合治疗各种癌症。CM369 IND申请将于2022年Q2提交。
公司运营稳健 加速产业布局
■ 为满足公司持续增长的研发、临床、生产、运营及产品商业化需求,公司通过加速人才储备、优化人才政策打造一支高竞争力的人才队伍。截止2021年底,公司拥有逾320位员工,同比增长154%;
■ 除成都总部,康诺亚在北京、上海、广州、武汉等多地设立办公室;
■ 占地113亩、高标准、国际化的新商业规模基地一期建设于2021年底封顶,目前已进入机电安装阶段,将于2022年建成8条2000升的抗体原液生产线和2条制剂生产线。首条生产线预计于2022年年中试运营。
合作深化再升级 共同探索前瞻性领域
■ 2021年康诺亚积极展开对外合作。公司与石药集团先后就CM310及CM326在中重度哮喘和COPD等呼吸系统疾病适应症的中国(不包括香港、澳门和台湾地区)权益达成合作。双方亦在神经退行性疾病领域达成战略联盟,共同确定、研究、开发和商业化一种或多种神经系统疾病产品。
■ 2021年9月与诺诚健华签订战略合作协议,进一步深化双方研发合作,致力于开发first-in-class大分子创新药造福患者。
获资本市场高度关注与认可
康诺亚自成立起就备受资本市场关注,公司于2021年3月完成C轮融资,共计筹集1.3亿美金,并于7月在香港联合交易所主板上市,共计筹集35.7亿港币。
今年3月,公司正式获纳港股通,再次印证资本市场对公司研发能力和业务发展的充分肯定。
未来康诺亚将继续以临床未尽之需为导向,持续高效推进创新药物发展;提速商业化基地建设,将创新实力尽快转化为临床价值,为患者提供更多治疗选择,让高质量、可负担的国产创新药尽快惠及中国患者。