18周EASI-75应答率达73.9%!司普奇拜单抗青少年特应性皮炎III期临床数据重磅亮相EADV 2025!
公司要闻
•2025年09月22日
2025年9月17-20日,第34届欧洲皮肤病与性病学会(EADV)大会在法国巴黎举行,本届大会上,由北京大学人民医院张建中教授团队牵头的一项多中心、随机、双盲、安慰剂对照Ⅲ期临床研究(NCT06277765)公布了最新成果1,该研究聚焦于司普奇拜单抗治疗青少年中重度特应性皮炎(AD)的疗效与安全性,不仅为临床实践提供了新的循证证据,也为广大青少年AD患者带来了新的曙光。
01
从成人到青少年:
司普奇拜单抗再获突破
司普奇拜单抗是一种全新人源化单克隆抗体,可精准靶向IL-4受体α亚基(IL-4Rα),同时阻断 IL-4 和 IL-13 两种关键细胞因子的信号传导,从而有效缓解AD疾病症状2,3。与度普利尤单抗不同,司普奇拜单抗依赖空间表位与靶点结合,此表位与IL-4/IL-13结合位点邻近甚至重合,继而在阻断IL-4Rα信号传导方面表现更优4。目前,司普奇拜单抗已在中国获批用于成人中重度AD的治疗。尽管在成人群体中疗效确切,但针对青少年AD患者的循证证据仍相对缺乏。因此,司普奇拜单抗用于青少年患者的Ⅲ期研究结果自启动以来便备受学界与临床关注。
该项Ⅲ期研究共纳入180例12岁≤年龄<18岁的青少年患者,以2:1比例随机分配至司普奇拜单抗组(n=120)或安慰剂组(n=60),双盲治疗周期为18周,并根据患者体重制定给药方案(图1)。共同主要终点设定为第18周时EASI评分较基线改善≥75%(EASI-75),以及IGA评分达到0或1分且较基线下降≥2分(IGA应答)。
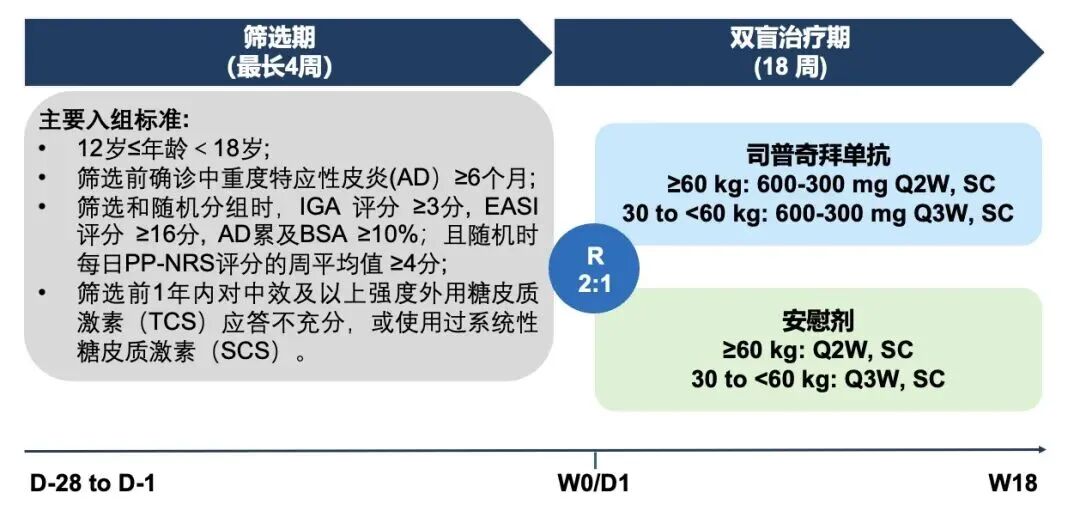
图1:研究设计
02
主要终点均达到:
司普奇拜单抗显著改善青少年患者皮损与瘙痒
治疗第18周,司普奇拜单抗组达共同主要终点,均显著优于安慰剂:
- EASI-75应答率:18周时,司普奇拜单抗组高达73.9%的患者实现EASI-75应答,显著高于安慰剂组(43.3%,P<0.0001)。(图2A)
- IGA应答率:18周时,司普奇拜单抗组IGA应答率高达 57.1%,显著优于安慰剂组(25.0%,P<0.0001),进一步验证了司普奇拜单抗在研究者整体评估中的疗效优势。(图2B)
- PP-NRS改善:司普奇拜单抗治疗第18周,PP-NRS较基线改善高达49.5%。(图2C)
上述结果一致表明,司普奇拜单抗在青少年中重度AD患者中同样能够实现强效的皮损改善与瘙痒缓解。
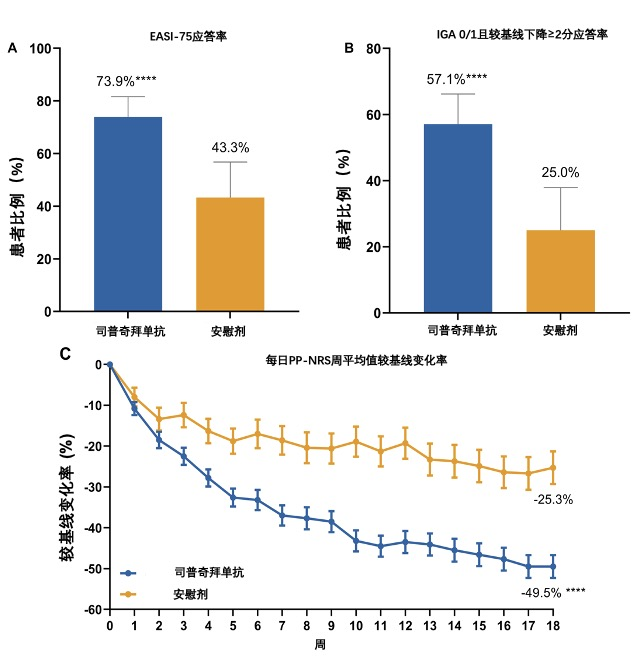
图2:司普奇拜单抗治疗18周患者改善:(A) EASI-75应答率;(B) IGA 0/1且较基线下降≥2分应答率;(C) 每日PP-NRS周平均值较基线变化率(****:P < 0.0001 vs. 安慰剂)
03
司普奇拜单抗
治疗青少年AD安全性与耐受性良好
安全性方面,司普奇拜单抗组与安慰剂组的治疗相关不良事件(TEAEs)发生率相当,且多为轻中度(表1)。最常见的不良事件为上呼吸道感染。值得关注的是,研究中未观察到结膜炎不良事件的发生。这一结果提示,司普奇拜单抗不仅疗效显著,而且在青少年人群中具有良好的安全性与耐受性,为青少年AD患者提供新的更加安全可靠的治疗选择。
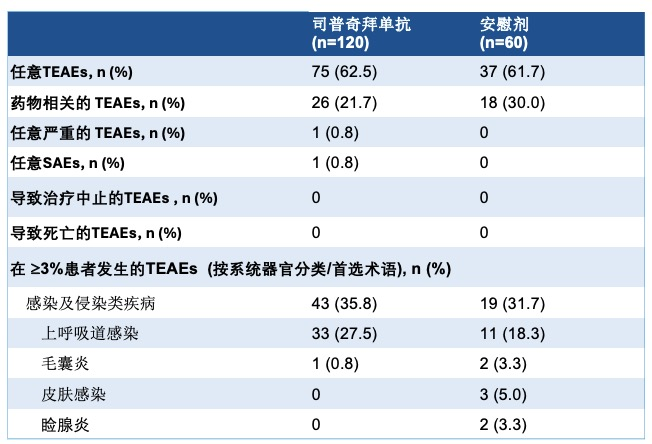
表1:安全性评估
本次EADV大会上公布的司普奇拜单抗青少年AD的Ⅲ期临床数据显示,司普奇拜单抗在青少年中重度特应性皮炎患者中展现出显著的疗效与良好的安全性,标志着该群体新型疗法的一项重要进展。
张建中 教授
北京大学人民医院皮肤科主任
“作为我国首个自主研发并成功获批上市的IL-4Rα单抗,司普奇拜单抗在中重度特应性皮炎治疗领域具有里程碑意义。本次EADV大会公布的青少年ADⅢ期临床研究18周数据进一步印证了其强效改善及安全可控的优势。期待未来积累更多真实世界研究和长期随访数据,为中重度AD的长期规范化管理提供更加坚实的循证支持。”
参考文献:
1. Zhang J, Zhang F, Wei A, Zhou C, Zhao Y, Chen B, Huang Y, Liu W. Efficacy and safety of stapokibart in adolescents with moderate-to-severe atopic dermatitis: A phase 3 trial. Poster presented at: 34th European Academy of Dermatology and Venereology (EADV) Congress; 2025 Sep; Paris, France. Poster P3253.
2. Zhao Y, Zhang L, Zhang J; CM310AD005 Study Investigators. Efficacy and safety of stapokibart (CM310) in adults with moderate-to-severe atopic dermatitis: A multicenter, randomized, double-blind, placebo-controlled phase 3 trial. J Am Acad Dermatol. 2024;91(5):984-986. doi:10.1016/j.jaad.2024.07.1447.
3. Zhao Y, Zhang L, Wu L, et al. Long-term efficacy and safety of stapokibart for moderate-to-severe atopic dermatitis: 52-week results from a phase 3 trial. Allergy. 2025;80(5):1348-1357. doi:10.1111/all.16368.
4. Zhao Y, Zhang L, Wu L, et al. Stapokibart Rapidly and Consistently Improves the Clinical Signs Across All Body Regions in Adults With Moderate-to-Severe Atopic Dermatitis. Int J Dermatol. 2025;64(10):1939-1941. doi:10.1111/ijd.17820.
