国家医保局解读2025年医保药品目录,司普奇拜单抗作为新增药品代表获认可
公司要闻
•2025年12月10日
为进一步增进社会公众对医保药品目录调整工作的认知与理解,国家医疗保障局于12月9日20:00在线播出2025年医保药品目录解读,详解2025年目录调整情况。解读会上,国家医疗保障局医药服务管理司相关领导和专家围绕目录调整概况、目录调整工作流程、医保目录调整各阶段产出,以及准备、申报、评审、测算、谈判/竞价阶段结果分析等展开解读,并对今年纳入的新增药品类型、治疗领域和特征进行深入分析。
在新增药品解读中,医保专家以5款创新药为例,解释本次新增纳入医保的药品,需具备“填补空白、同类更优、更具性价比” 优势特征。作为其中唯一一款自身免疫性疾病创新药,司普奇拜单抗被列为代表性药物获点评认可。专家在会上表示,“司普奇拜单抗是一个国产的1类新药,适应症是特应性皮炎等。进入医保之后,它能以更合理的价格,减轻社会的成本和医保基金的负担,同时,也更丰富了临床的选择,这也是国内药品实现了一定的进口替代。”
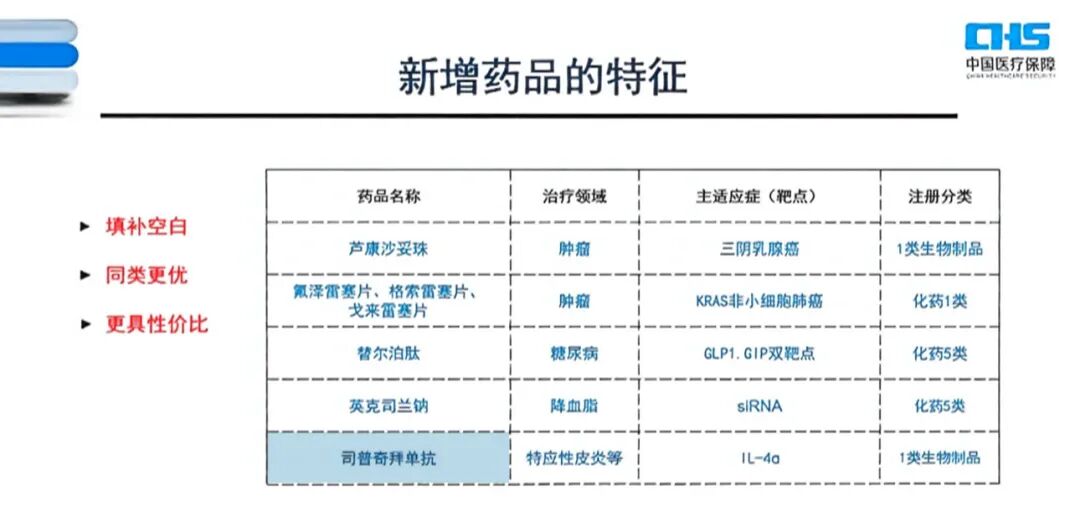
图源:2025年医保药品目录解读会
填补空白
此次纳入新版国家基本医疗保险药品目录,康悦达®(司普奇拜单抗)在多个适应症上填补治疗空白,具备开创性意义的“9项第一”:
■ IL-4Rα靶点首个以空间表位与靶点结合的源头创新药
■ 国内首个自主研发、全球唯二获批上市的IL-4Rα抗体药物
■ 国产首个治疗中重度特应性皮炎生物制剂
■ 中国首个治疗慢性鼻窦炎伴鼻息肉生物制剂
■ 全球首个治疗季节性过敏性鼻炎IL-4Rα抗体药物
■ 首个季节性过敏性鼻炎Ⅲ期临床研究结果发表于全球顶级期刊Nature Medicine,亦是全球范围内首次报告基于IL-4Rα靶点的生物制剂治疗季节性过敏性鼻炎研究成果
■ 首个慢性鼻窦炎伴鼻息肉Ⅲ期临床研究结果发表于全球顶级期刊JAMA,亦为中国鼻科领域创新药首登JAMA
■ 首个国内特应性皮炎III期临床研究结果发表于国际过敏与免疫学顶级期刊Allergy
■ 中国特应性皮炎患者样本量最大的III期临床研究
同类更优
康悦达®(司普奇拜单抗)通过精准靶向IL-4Rα,同时阻断 IL-4 和 IL-13 两种关键细胞因子的信号传导,有效缓解多种2型炎症疾病症状1,2。其依赖空间表位与靶点结合,此表位与IL-4/IL-13结合位点邻近甚至重合,继而在阻断IL-4Rα信号传导方面表现更优3。
治疗成人中重度特应性皮炎快速止痒、头颈部应答更快更强、强效清损、长期安全1-3,助力中国特应性皮炎诊疗标准迈向EASI-90新时代,为患者带来更优治疗选择。慢性鼻窦炎伴鼻息肉治疗能够快速显著缩小息肉、改善嗅觉、强效畅鼻4,改写现有治疗格局;季节性过敏性鼻炎治疗实现快速缓解鼻塞、持续改善鼻部和眼部过敏症状5,为传统治疗无效的中重度季节性过敏性鼻炎患者提供全新选择。相关研究发表于全球顶级期刊JAMA、Nature Medicine、Allergy,并被纳入《生物制剂治疗慢性鼻窦炎伴鼻息肉中国意见书》(2025)等权威推荐。
更高可及性
康悦达®(司普奇拜单抗)成功纳入新版国家基本医疗保险药品目录,将显著降低患者用药负担,让更多有需求的患者能够以可负担的价格获得创新治疗。康诺亚将通过本土化生产保障供应,确保创新药物的稳定供应。
康悦达®(司普奇拜单抗)预充式自动注射笔此次也同步纳入新版国家基本医疗保险药品目录,作为原有给药方式的升级版本,将以创新优化的设计,为患者提供更为便捷的治疗体验,推动疾病治疗向更友好、高效、长期的管理模式发展。
未来,康诺亚还将持续聚焦临床需求,坚持“真创新”、“差异化创新”理念,不断推出突破性解决方案,助力患者拥有更加健康、高质量的生活。
参考文献:
1. Zhao Y, Zhang L, Zhang J, et al. Efficacy and safety of stapokibart (CM310) in adults with moderate-to-severe atopic dermatitis: A multicenter, randomized, double-blind, placebo-controlled phase 3 trial. J Am Acad Dermatol. 2024;91(5):984-986. doi:10.1016/j.jaad.2024.07.1447.
2. Zhao Y, Zhang L, Wu L, et al. Long-term efficacy and safety of stapokibart for moderate-to-severe atopic dermatitis: 52-week results from a phase 3 trial. Allergy. 2025;80(5):1348-1357. doi:10.1111/all.16368.
3. Zhao Y, Zhang L, Wu L, et al. Stapokibart Rapidly and Consistently Improves the Clinical Signs Across All Body Regions in Adults With Moderate-to-Severe Atopic Dermatitis. Int J Dermatol. 2025;64(10):1939-1941. doi:10.1111/ijd.17820.
4. Shen Shen et al., Stapokibart for severe uncontrolled chronic rhinosinusitis with nasal polyps: the CROWNS-2 randomized clinical trial. JAMA. 2025 Aug 18:e2512515.
5. Zhang Y, Luo Zhang et al. Stapokibart for moderate-to-severe seasonal allergic rhinitis: a randomized phase 3 trial. Nat Med. 2025 Jul;31(7):2213-2221.
